La thérapie génique – une vraie révolution médicale
Réparer, ou remplacer, un gène défectueux pour corriger les erreurs de la Nature, c’est la promesse de la thérapie génique. Génératrice d’espoirs les plus fous, cette nouvelle approche médicale, jugée aussi révolutionnaire que la vaccination ou la découverte des antibiotiques en leur temps, se heurte toutefois à des problèmes techniques, mais aussi éthiques.
Principe
Depuis l’établissement, en 1993, de la cartographie du génome humain et son décryptage en 2003, on connaît de mieux en mieux le fonctionnement des gènes et notamment, quel gène-code s’associe à quelle protéine et à quelle fonction du corps il se rapporte.
Une première française
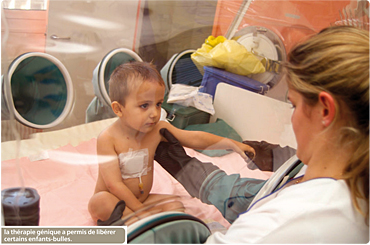
Mais c’est en 1999 que le professeur Alain Fischer, chercheur à l’Inserm (Institut national scientifique d’études et de recherches médicales) a démontré la puissance de cette technique, et le formidable espoir qu’elle pouvait engendrer, en réalisant – à l’hôpital Necker (Paris) – le premier essai de thérapie génique, couronné de succès, sur l’être humain. Il a travaillé avec un groupe d’enfants atteints d’une maladie génétique qui rendait leur système immunitaire déficient (déficit immunitaire combiné sévère lié au chromosome x ou dics-x). Ces enfants étaient contraints de vivre sous bulle, dans une atmosphère totalement stérile. L’équipe du professeur Fischer a isolé le gène en cause avant de prélever, sur les patients, des cellules souches (cellules capables de se transformer en plusieurs types de cellules). Puis, en laboratoire, un gène sain a été introduit dans ces cellules avant de les réinjecter dans les organismes des enfants : les dix jeunes patients traités ont pu sortir de leur bulle. Toutefois, deux d’entre eux ont développé une leucémie et un seul a pu être sauvé. Cette tragédie a entraîné une suspension des essais sur l’homme entre 2002 et 2004 mais, devant un tel taux de réussite, 98 %, ils ont repris très vite. Les chercheurs ont ainsi pu identifier les raisons pour lesquelles ces deux enfants – et pas les autres – avaient déclenché des cancers : dans leur organisme, le gène-médicament s’est implanté à proximité de celui qui gère la production des globules rouges et des lymphocytes. Un « accident » qui peut être prévenu par les praticiens.
 Concept
Concept
Dès lors, on peut imaginer soigner en utilisant les gènes de deux façons distinctes :
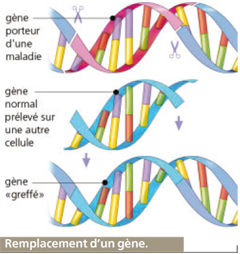
Le remplacement
Même si le concept est séduisant, remplacer un gène déficient par un gène sain reste aujourd’hui le projet thérapeutique le plus difficile, d’un point de vue technique, à mettre en place.
L’apport thérapeutique
Il s’agit ici d’utiliser le gène comme un médicament capable de coder une protéine pour amener celle-ci à déclencher des effets contrebalançant ceux, néfastes, du gène malade.
Fonctionnement
Identification du gène déficient
C’est évidemment la première étape. Devant une affection donnée, congénitale ou acquise, il faut déterminer quels sont les gènes impliqués. Une fois cette identification effectuée, les chercheurs isolent un gène-médicament et le clonent en laboratoire.
Implatation du gène-remède
Pour introduire le gène-médicament dans la cellule infectée, les scientifiques utilisent un vecteur. Le plus souvent, il s’agit d’un rétrovirus car celui-ci a la faculté de migrer et de transverser la membrane cytoplasmique pour atteindre le noyau des cellules de certains organes. Il y a alors réplication de son ADN, ou son de ARN, à l’intérieur de la cellule et, lorsque celle-ci se reproduit, elle le fait avec les propriétés du virus. C’est le mécanisme de l’infection.
Dans le cadre de la thérapie génique, on manipule le virus de manière à le rendre inoffensif puis on remplace son ADN (ou ARN) par celui d’un gène-médicament qui contrôle la production d’une protéine spécifique afin d’induire un effet thérapeutique.
Une infection soignante
Ensuite, le virus va pénétrer la cellule-cible et utilisera le pouvoir de réplication de celle-ci de manière à « infecter » d’autres cellules et leur conférer ainsi les propriétes thérapeutiques du gène-médicament.
Atteinte de la cellule-cible
Les généticiens disposent de trois techniques pour s’assurer que le virus atteigne la bonne cellule-cible et éviter les conséquences désastreuses des premiers essais :
• In vivo. Le virus est introduit dans la circulation sanguine par une banale piqûre avant d’être transporté, par le sang, jusqu’aux cellules-cibles.
• In situ. Dans ce cas, on introduit directement le vecteur modifié dans l’organe concerné.
• In vitro. On prélève, sur un malade, les cellules à modifier et on y introduit , en laboratoire, le virus porteur du gène-médicament. Les cellules transformées sont ensuite réinjectées dans les tissus du patient.